Nguyên tử khối là gì? Nguyên tử khối trung bình là gì? Nguyên tử khối có quan trọng không? Cách tính nguyên tử khối như thế nào? Đó là một số câu hỏi được gửi về cho LabVIETCHEM trong thời gian gần đây. Và để hiểu rõ hơn về nguyên tử khối, các bạn hãy cùng chúng tôi đón đọc nội dung dưới đây nhé.
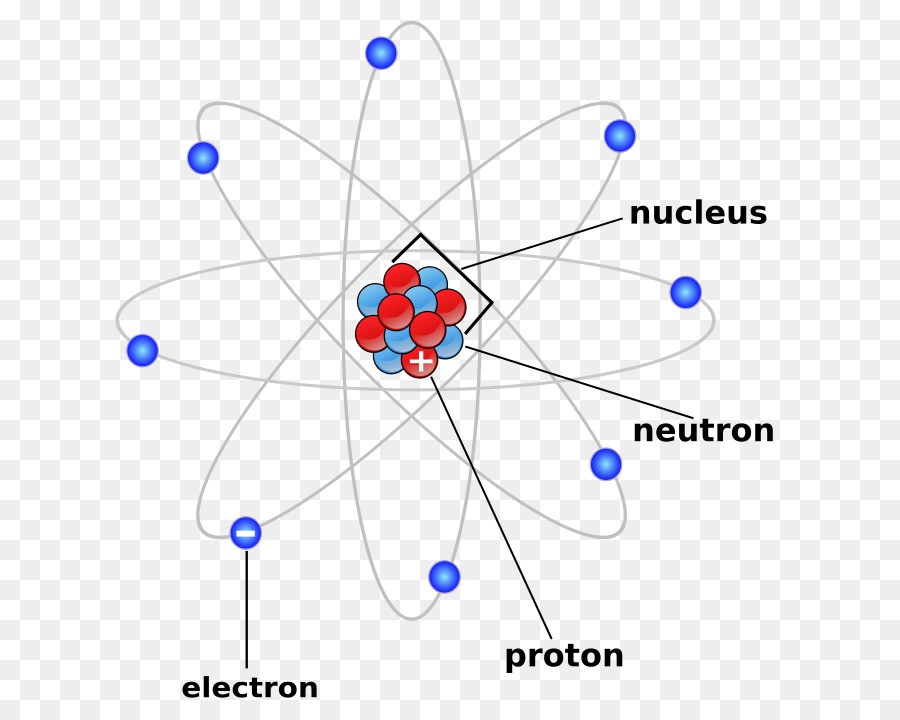
Nguyên tử khối là gì
Nguyên tử khối là khối lượng tương đối của nguyên tử, tức là tổng khối lượng của proton, neutron và electron. Vì khối lượng của electron rất nhỏ nên nguyên tử khối chính là khối lượng của hạt nhân.
Đơn vị của nguyên tử khối là đơn vị cacbon (đvC). 1 đvC được tính bằng 1/12 khối lượng của một nguyên tử cacbon. Khối lượng của một nguyên tử cacbon là 1,6605 . 10 -24 g => 1đvC = (1/12). 1,9926.10 -23 = 1,6605.10 -24 g.
Mỗi nguyên tố có số proton và neutron khác nhau nên nguyên tử khối của chúng cũng khác nhau. Khối lượng nguyên tử có trị số vô cùng nhỏ và được tính bằng g hoặc kg.
Phân tử khối là khối lượng của một nguyên tử được tính bằng đvC và nó được xác định là tổng nguyên tử khối của các nguyên tử trong phân tử chất đó. Ví dụ như phân tử khối của khí oxy O2 bằng 16.2 = 32 đvC.
Phần lớn các nguyên tố hóa học đều là hỗn hợp của nhiều đồng vị với tỉ lệ phần trăm số nguyên tử xác định. Do đó, nguyên tử khối của các nguyên tố có nhiều đồng vị được xác định là nguyên tử khối trung bình của hỗn hợp các đồng vị đó có tính đến tỉ lệ phần trăm số nguyên tử tương ứng.
Giả sử nguyên tố X có 2 đồng vị là A và B. Kí hiệu A và B lần lượt là nguyên tử khối của 2 đồng vị với tỉ lệ phần trăm số nguyên tử tương ứng là a và b. Khi đó nguyên tử khối trung bình Atb của nguyên tố X là: Atb = (a.A + b.B)/100
Trong những phép toán không đòi hỏi độ chính xác cao thì chúng ta có thể coi nguyên tử khối chính bằng số khối.

Căn cứ vào nguyên tử khối của một chất, chúng ta sẽ biết được đó là chất nào. Ngoài ra, nó cũng là yếu tố cần biết trong những bài toán lập công thức hóa học của hợp chất và những bài tập liên quan đến tính toán hóa học. Biết được nguyên tử khối của càng nhiều chất thì việc giải các bài tập hóa học sẽ đơn giản hơn.
Bảng nguyên tử khối của các chất thường gặp:
|
Số Proton |
Ký hiệu hoá học |
Nguyên tử khối |
Hoá trị |
|
1 |
H |
1 |
I |
|
6 |
C |
12 |
IV, II |
|
7 |
N |
14 |
III,II,IV,.. |
|
8 |
O |
16 |
II |
|
9 |
F |
19 |
I |
|
11 |
Na |
23 |
I |
|
12 |
Mg |
24 |
II |
|
13 |
Al |
27 |
III |
|
14 |
Si |
28 |
IV |
|
15 |
P |
31 |
III, V |
|
16 |
S |
32 |
II,IV,VI,.. |
|
17 |
Cl |
35,5 |
I,.. |
|
19 |
K |
39 |
I |
|
20 |
Ca |
40 |
II |
|
26 |
Fe |
56 |
II,III |
|
29 |
Cu |
64 |
I,II |
|
30 |
Zn |
65 |
II |
|
35 |
Br |
80 |
I,… |
|
47 |
Ag |
108 |
I |
|
56 |
Ba |
137 |
II |
|
80 |
Hg |
201 |
I,II |
|
82 |
Pb |
207 |
II,IV |
Cacbon được lựa chọn là đơn vị tiêu chuẩn để đo khối lượng nguyên tử. Đơn vị cacbon được ký hiệu là đvC và có khối lượng bằng 1/12 khối lượng của nguyên tử cacbon. Vậy tại sao lại lựa chọn đơn vị cacbon làm đơn vị đo khối lượng chuẩn của nguyên tử?
Trên thực tế thì vào thế kỷ thứ XII, các nhà khoa học đã từng sử dụng hydro và oxy để làm đơn vị chuẩn của nguyên tử. Tuy nhiên, sau nhiều nghiên cứu, các nhà khoa học đã chứng minh được rằng, hydro và oxy có sai số lớn hơn đơn vị cacbon. Do đó, vào năm 1961, Viện đo lường Quốc tế đã thống nhất và lựa chọn đơn vị cacbon để làm đơn vị cho nguyên tử khối. Nguyên nhân là vì sự phổ biến của nguyên tử này trong tự nhiên cũng như nó có độ sai số thấp hơn hydro và oxy.
Do đó đến thời điểm hiện tại, khối lượng của nguyên tử cacbon trở thành khối lượng đo lường nguyên tử khối chuẩn quốc tế.

Khối lượng nguyên tử được tính như thế nào
Bước 1: Nhớ rõ 1đvC = 1,6605.10-27 kg =1,6605.10-24 g
Bước 2: Tra bảng nguyên tử khối của các nguyên tố hóa học . Ví dụ như nguyên tố A có nguyên tử khối là a, tức A = a.
Bước 3: Khối lượng thực của nguyên tử A là: mA = a . 0,166 .10-23 g
Khối lượng thực của nguyên tử A là: mA = a . 0,166.10 -23 g
Ví dụ như: Cho 16g oxy. Hãy xác định số nguyên tử oxy có trong 16g oxy và tính khối lượng của một nguyên tử oxy.
Hướng dẫn giải:
Áp dụng công thức tính nguyên tử khối, ta có:
Số nguyên tử = Khối lượng tính bằng g/Khối lượng tính bằng g của 1 nguyên tử
=> Số nguyên tử trong 16g oxi được xác định là: 16/(16.1,6605.10-24) = 6,02.10-23
1mol oxi có khối lượng 16g = 16(đvC) thì 1 nguyên tử oxi sẽ có khối lượng là 16.1,6605.10 -24 g
Bảng nguyên tử khối của các nguyên tố hóa học
Cách 1:
Anh hydro là một
Mười hai cột cacbon
Nito mười bốn tròn
Oxy mỏi mòn mười sáu
Natri hay láu táu
Nhảy tót lên hai ba
Khiến Magie gần nhà
Ngậm ngùi đành hai bốn
Hai bảy nhôm la lớn
Lưu huỳnh giành ba hai
Khác người thật là tài
Clo ba lăm rưỡi
Kali thích ba chín
Canxi tiếp bốn mươi
Năm lăm mangan cười
Sắt đây rồi năm sáu
Sáu tư đồng nổi cáu
Bởi kém kẽm sáu lăm
Tám mươi Brom nằm
Xa bạc trăm lẻ tám
Bari lòng buồn chán
Một ba bảy ích chi
Kém người ta còn gì
Hai lẻ bảy bác chì
Thủy ngân hai lẻ một
Cách 2:
Hai ba Natri
Nhớ ghi cho rõ
Kali chẳng khó
Ba chín dễ dàng
Khi nhắc đến Vàng
Một trăm chín bảy
Oxy gây cháy
Chỉ mười sáu thôi
Còn Bạc dễ rồi
Một trăm lẻ tám
Sắt màu trắng xám
Năm sáu có gì
Nghĩ tới Beri
Nhớ ngay là chín
Gấp ba lần chín
Là của anh Nhôm
Còn của Crôm
Là năm hai đó
Của Đồng đã rõ
Là sáu mươi tư
Photpho không dư
Là ba mươi mốt
Hai trăm lẻ một
Là của Thủy Ngân
Chẳng phải ngại ngần
Nito mười bốn
Hai lần mười bốn
Silic phi kim
Can xi dễ tìm
Bốn mươi vừa chẵn
Mangan vừa vặn
Con số năm lăm
Ba lăm phẩy năm
Clo chất khí
Phải nhớ cho kỹ
Kẽm là sáu lăm
Lưu huỳnh chơi khăm
Ba hai đã rõ
Chẳng có gì khó
Cacbon mười hai
Bari hơi dài
Một trăm ba bảy
Phát nổ khi cháy
Cẩn thận vẫn hơn
Khối lượng giản đơn
Hydro là một
Còn cậu Iot
Ai hỏi nói ngay
Một trăm hai bảy
Nếu hai lẻ bảy
Lại của anh Chì
Brôm nhớ ghi
Tám mươi đã tỏ
Nhưng vẫn còn đó
Magie hai tư
Chẳng phải chần trừ
Flo mười chín
Vậy là labvietchem.com.vn đã giúp các bạn giải đáp được thắc mắc nguyên tử khối là gì cũng như cách tính, mẹo học nguyên tử khối của các nguyên tố. Hy vọng rằng với những kiến thức này, các bạn đã sẽ vận dụng một cách hiệu quả trong việc giải các bài tập hóa học.
Xem thêm:
Hỗ trợ

Nguyễn Văn Trọng
Sales Director
094 6688 777
trongnguyen@labvietchem.vn

Cao Thu Hoài
Sales Engineer
0325 290 685
thietbi404@labvietchem.vn

Nguyễn Thúy Hảo
Sales Engineer
0364 841 980
nguyenhao@labvietchem.com.vn

Vũ Thị Thư
Sales Engineer
0326 046 889
vuthu@labvietchem.com.vn

Trần Thị Kim Mỵ
Sales Engineer
0348 140 389
sales@labvietchem.com.vn

Trịnh Văn Hường
Sales Engineer
0986 768 834
sales@labvietchem.com.vn

Lưu Vân Quỳnh
Trưởng nhóm sinh hóa
0367 631 984
sales@labvietchem.com.vn

Phan Hải Phong
Sales Engineer
0949 966 821
sales@labvietchem.com.vn

Dương Tuấn Anh
Sales Engineer
0329 422 268
sales@labvietchem.com.vn

Hotline
Hóa chất và thiết bị thí nghiệm
0826 050 050
saleadmin806@vietchem.vn

Hồ Thị Hoài Thương
Sales Engineer
0967 609 897
kd801@labvietchem.vn

Phạm Thị Nhật Hạ
Sales Engineer
0985 357 897
kd803@vietchem.vn

Vũ Thị Kim Khánh
Sales Engineer
0965 948 897
kd802@vietchem.vn

Nguyễn Hoàng Giáo
Sales Engineer
0939 154 554
kd201@labvietchem.com.vn

Tạ Thảo Cương
Sales Engineer
0888851646
kd205@labvietchem.vn

Trần Thị Trúc Lil
Sales Engineer
0325 300 716
kd202@labvietchem.com.vn

Trần Dương Thanh
Nhân viên kinh doanh
0964980951
saleadmin201@labvietchem.vn
Phép tính tính Số nguyên tử trong 16g oxi ở bước ba trên là sai rồi bạn ơi. Hãy xem lại
Phép tính tính Số nguyên tử trong 16g oxi ở bước ba trên là sai rồi bạn ơi. Hãy xem lại
Nhận xét đánh giá