Andehit axetic là gì? Nó được tìm thấy như thế nào và có cách điều chế, tính chất ra sao? Bài viết dưới đây sẽ giúp bạn hiểu rõ hơn về ứng dụng cũng như các đặc điểm đặc trưng của chúng, hãy cùng theo dõi ngay nhé.
Andehit axetic hay axetandehit (ethanal) là một trong những aldehyde quan trọng nhất, tồn tại phổ biến trong tự nhiên và được sản xuất ở quy mô lớn trong công nghiệp.
Andehit axetic có công thức là CH3CHO, đôi khi cũng thường được viết thành MeCHO (Me tương ứng với methyl).
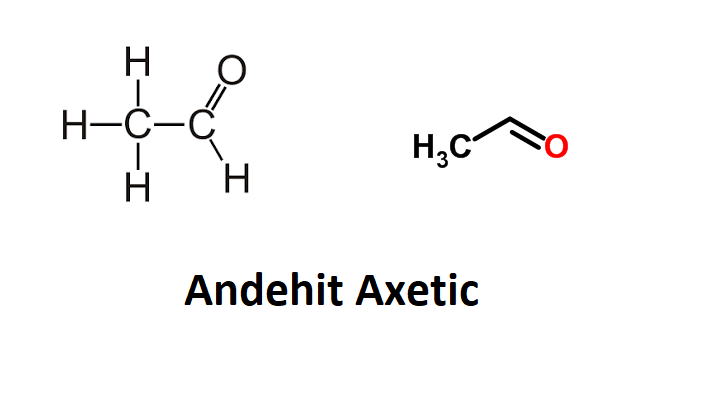
Andehit axetic là gì?
Andehit axetic có công thức hóa học CH3CHO hoặc C2H4O
Tạo ra bạc, amoni nitrat và amoni axetat khi cho tác dụng với bạc nitrat và amoniac
4AgnO3 + CH3CHO + 5NH3 → 4Ag + 3CH3COONH4 + 3NH4NO3
Phản ứng với CuOH2 thu được axit axetic và nước, đồng (I) oxit
2CH3CHO + Cu(OH)2 → CH3COOH + Cu2O + 2H2O
Khi phản ứng với đồng (II) oxit và natri hidroxit cho ra natri axetat, nước và đồng (I) oxit
CH3CHO + NaOH + 2Cu(OH)2 → CH3COONa + 3H2O + Cu2O
CH3CHO + H2 → CH3CH2OH
Andehit axetic có thể được điều chế từ axetilen, ancol etylic,…
C2H4 + O2 → CH3CHO + H2O (có sự tham gia của chất xúc tác HgCl2 và nhiệt độ)
C2H2 + H2O → CH3CHO (nhiệt độ, HgSO4)
C2H5OH + CuO → CH3CHO + H2O + Cu (nhiệt độ)
CH3COOH + H2 → CH3CHO + H2O (chất xúc tác và nhiệt độ)
CH3COOC2H3 + NaOH → CH3COONa + CH3CHO + H2O (điều kiện nhiệt độ)
Ngoài ra còn có thể thông qua quá trình lên men sữa chua để tạo thành CH3CHO
Điều chế andehit axetic như thế nào?
2CH3CHO + Cu(OH)2 → CH3COOH + 2H2O + Cu2O

Bài tập vận dụng về andehit axetic
Bài tập 1: Hãy trình bày phương pháp hóa học để phân biệt các dung dịch: anđehit axetic, glixerol, axetic, ancol etylic
Lời giải:
Cách phân biệt
CH3CHO: Cu(OH)2 nhiệt độ thường sau đó tiến hành đun nóng
CH3COOH: Sử dụng Cu(OH)2 ban đầu không có hiện tượng nhưng sau khi đun nóng sẽ xuất hiện kết tủa màu đỏ gạch
C3H5(OH)2: hóa hồng quỳ tím
C2H5OH: tạo ra dung dịch màu xanh lam khi tác dụng với cu9OH)2 ở nhiệt độ thường
Bài tập 2: Sau khi dẫn hỗn hợp khí X bao gồm axetilen cùng andehit axetic vào dung dịch AgNO2 trong amoniac ta được kết tủa gồm hai chất. Lấy kết tủa này cho vào dung dịch axit HCl dư thấy có hiện tượng khí bay lên và còn một phần không tan Y. Tiến hành hòa tan Y vào trong dung dịch HNO3 đặc thấy có khí màu nâu bay lên. Giải thích quá trình thí nghiệm trên bằng cách viết các phương trình hóa học.
Lời giải:
Các phương trình phản ứng trong thí nghiệm trên:
CH≡CH + 2AgNHO3 + 2NH3 → AgC≡CAg + 2NH4NO3
CH3CHO + 2AgNO3 + H2O + 2NH3 → CH3COONH4 + 2NH4NO3 + 2Ag
Lọc kết tủa AgC≡CAg và Ag cho vào dung dịch HCl thì chỉ có AgC≡CAg phản ứng
AgC≡CAg + 2HCl → HC≡CH + 2AgCl
Phần không tan chính là Ag và AgCl, hòa tan vào trong HNO3 thì chỉ có Ag phản ứng
Ag + 2HNO3 → AgNO3 + NO2 + H2O
Bài tập 3: Cho hỗn hợp A với khối lượng 10 gam bao gồm axit axetic và anđehit axetic. Tiến hành cho A tác dụng với lượng dư AgN3 trong dung dịch amoniac thu được 21,6 gam Ag kết tủa. Để trung hòa A cần đến V ml dung dịch NaOH 0,20M
a) Viết các phương trình hóa học của các phản ứng đã xảy ra trên
b) Hãy tính phần trăm khối lượng của mỗi chất có trong A và thể tích dung dịch NaOH đã sử dụng.
Lời giải:
a) Các PTPƯ:
CH3CHO + 3NH3 + 2AgNO3 + H2O → CH3COONH4 + 2NH4NO3 + 2Ag (1)
CH3COOH + NaOH → H2O + CH3COONa (2)
b) Từ bài ra, ta có: nAg = 21,6/108 = 0,2 mol
Theo phương trình phản ứng (1) thì nCH3CHO = 1/2nAg = 0,2/2 = 0,1 ml
Vậy khối lượng của CH3CHO là mCH3CHO = 0,1 x 44 = 4,4 gam
=> %CH3CHO = 4,4/10 x 100% = 44%
=> %CH3COOH = 100 – 44 = 66%
=> Khối lượng của CH3COOH là: mCH3COOH = 10 -4,4 = 5,6 gam
=> nCH3COOH = 5,6/60 = 0,0933 mol
Theo phương trình phản ứng (2), ta được: nNaOH = nCH3COOH = 0,0933 mol
Vậy VnaOH = 0,0933/0,2 = 4,665 lít
Trên đây là những thông tin cơ bản về andehit axetic là gì và một số bài tập vận dụng giúp bạn dễ nhớ hơn. Nếu vẫn còn thắc mắc bất cứ vấn đề nào liên quan hay muốn chia sẻ thêm các thông tin khác, bạn đọc hãy gọi ngay đến hotline 0826 020 020 hoặc để lại bình luận ngay dưới bài viết để LabVIETCHEM được biết và hỗ trợ bạn sớm nhất nhé.
Hỗ trợ

Tống Duy Cương
Director
0915 989 780
DuyCuong@labvietchem.vn

Nguyễn Văn Trọng
Deputy Director
094 6688 777
trongnguyen@labvietchem.vn

Cao Thu Hoài
Sales Engineer
0325 290 685
thietbi404@labvietchem.vn

Nguyễn Thúy Hảo
Sales Engineer
0364 841 980
nguyenhao@labvietchem.com.vn

Trần Thị Kim Mỵ
Sales Engineer
0348 140 389
sales@labvietchem.com.vn

Trịnh Văn Hường
Sales Engineer
0986 768 834
sales@labvietchem.com.vn

Lưu Vân Quỳnh
Trưởng nhóm sinh hóa
0367 631 984
sales@labvietchem.com.vn

Phan Hải Phong
Sales Engineer
0949 966 821
sales@labvietchem.com.vn

Dương Tuấn Anh
Sales Engineer
0329 422 268
sales@labvietchem.com.vn

Hotline
Hóa chất và thiết bị thí nghiệm
0826 050 050
saleadmin806@vietchem.vn

Hồ Thị Hoài Thương
Sales Engineer
0967 609 897
kd801@labvietchem.vn

Phạm Thị Nhật Hạ
Sales Engineer
0985 357 897
kd803@vietchem.vn

Vũ Thị Kim Khánh
Sales Engineer
0965 948 897
kd802@vietchem.vn

Nguyễn Hoàng Giáo
Sales Engineer
0939 154 554
kd201@labvietchem.com.vn

Tạ Thảo Cương
Sales Engineer
0888851646
kd205@labvietchem.vn

Trần Thị Trúc Lil
Sales Engineer
0325 300 716
kd202@labvietchem.com.vn

Trần Dương Thanh
Nhân viên kinh doanh
0964980951
saleadmin201@labvietchem.vn
Nhận xét đánh giá