Trong công nghiệp, khí Sunfurơ - SO2 có thể ứng dụng trong nhiều khía cạnh khác nhau. Tuy nhiên, đối với hệ sinh thái cũng như sức khỏe của con người, loại khí này có thể gây ra không ít những tác động tiêu cực. Hãy cùng LabVietChem tìm hiểu sơ bộ các thông tin về đặc trưng lý – hóa cũng như ứng dụng của Sunfurơ.
SO2 là chất gì? SO2 là một loại khí được tạo ra sau quá trình đốt cháy lưu huỳnh có chứa trong các loại nhiên liệu hóa thạch hoặc các loại quặng. Tên gọi khác của khí SO2 là Lưu huỳnh đioxit, Sulfur đioxit, khí Sunfurơ.
SO2 còn được gọi là Lưu huỳnh đioxit
Trong phân tử SO2 tồn tại 1 liên kết đôi S=O cũng như 1 liên kết đơn S-O. Do vậy, công thức cấu tạo của SO2 như sau:
O=S-O hoặc O-S=O
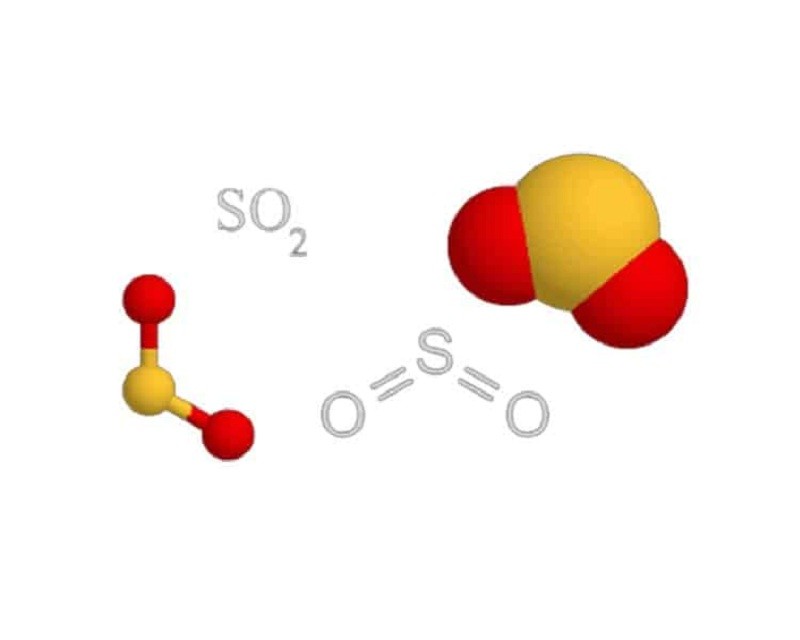
Công thức cấu tạo của SO2
Khí SO2 có các tính chất đặc trưng như sau:
SO2 là khí vô cơ độc, không màu và có khối lượng riêng nặng hơn không khí. Tính chất cơ bản của SO2 là làm vẩn đục nước vôi trong, làm mất màu cánh hoa hồng và dung dịch Brom.
Khối lượng phân tử SO2 là 64 amu, trọng lượng riêng là 2.551 g/l. Nhiệt độ nóng chảy đạt -72 độ C, nhiệt độ sôi đạt -10 độ C.
Vậy về cảm quan, khí SO2 có mùi hắc đặc trưng rất khó chịu. Đồng thời, khả năng tan trong nước của hợp chất này cũng rất tốt.
Về tính chất hóa học, SO2 có đầy đủ các đặc trưng của một oxit axit, vừa có thể đóng vai trò của chất khử, vừa hoạt động như một chất oxi hóa. Cụ thể như sau:
SO2 + H2O → H2SO3
SO2 + Na2O → Na2SO3
SO2 + 2NaOH → Na2SO3 + H2O
Khí SO2 được sinh ra trong quá trình đốt cháy các loại hóa thạch và quặng. Do vậy, khi có hiện tượng núi lửa phun trào, lượng SO2 thải ra ngoài không khí có thể đạt đến hàng triệu tấn.
Tuy nhiên, trong thí nghiệm và đời sống sản xuất công nghiệp thực tế, việc điều chế SO2 có thể thực hiện theo các phương pháp sau:
Quá trình phản ứng hóa học giữa axit Sunfuric H2SO4 và Na2SO3 ra SO2 chính là phương thức điều chế ra khí SO2 dùng trong các phòng thí nghiệm. Phương trình hóa học của phản ứng như sau:
Na2SO3 + H2SO4 → Na2SO4 + H2O + SO2↑
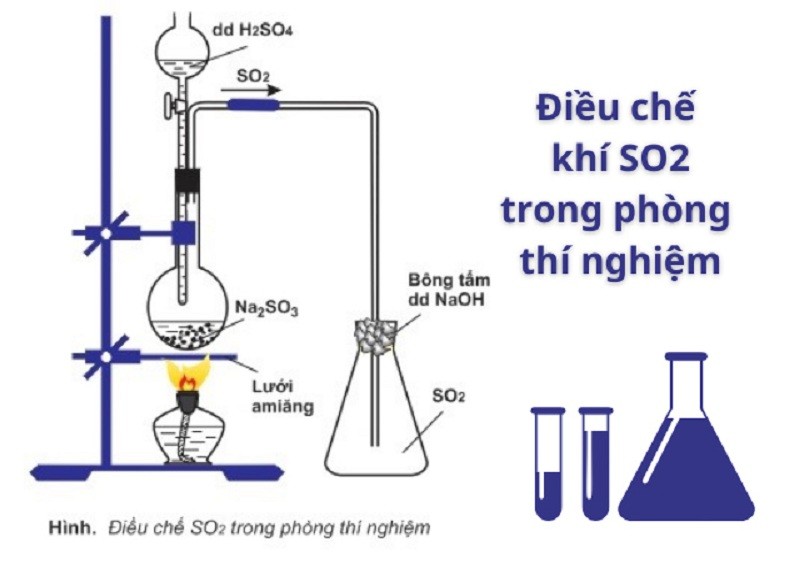
Điều chế SO2 trong phòng thí nghiệm
Có 2 cách để thu được khí SO2 phục vụ cho công nghiệp như sau:
Đốt cháy lưu huỳnh: S + O2 (t°) → SO2
Đối quặng pirit sắt: 4FeS2 + 11O2 → 2Fe2O3 + 8SO2↑
Trong đời sống, ứng dụng của SO2 rất đa dạng, có thể kể đến như:

SO2 có ứng dụng làm chất bảo quản hoa quả khô
Xét về bản chất, khí SO2 mang tính độc. Đối với cả con người và môi trường sinh thái, sự tồn tại của SO2 nếu vượt quá nồng độ cho phép có thể dẫn đến nhiều tác hại khôn lường.
Khi con người tiếp xúc trực tiếp với khí SO2, hít loại khí độc này vào cơ thể sẽ gây ra các triệu chứng khó chịu. Ví dụ như nóng rát đường mũi, cổ họng, tức ngực khó thở, choáng váng, mệt mỏi…
Nếu không tránh khỏi nguồn khí SO2 ngay và kịp thời có các biện pháp hỗ trợ y tế thì nguy cơ mắc phải các bệnh lý về đường hô hấp là rất cao. Bao gồm viêm đường hô hấp, viêm phổi… Thậm chí, trong nhiều trường hợp còn xác định, khí SO2 là nguyên nhân gây ra tình trạng viêm mắt nghiêm trọng cho con người.
Không chỉ vậy, khí SO2 khi kết hợp với nước và oxy sẽ hình thành nên axit Sunfuric – một loại axit mạnh rất độc hại. Nếu như chất này vô tình đi vào cơ thể con người sẽ gây ra rất nhiều hệ lụy nguy hiểm. Ví dụ như làm ảnh hưởng đến lượng kiềm dự trữ trong máu, cản trở quá trình chuyển hóa đường cũng như protein của cơ thể. Từ đó, gây ra hiện tượng tắc nghẽn mạch máu và nhiều bệnh lý khác.
Với môi trường sinh thái, khí SO2 cũng là một mối nguy hại không hề nhỏ. Nếu tồn tại với nồng độ cao, dư lượng lớn có thể gây ra nhiều tình huống bất cập. Ví dụ như các trận mưa axit làm các công trình sắt thép bị ăn mòn, cây cối hoa màu bị phá hủy…
Việc xử trí khí SO2 là cần thiết, đảm bảo tốt nhất cho sức khỏe con người và sự phát triển bình thường của hệ sinh thái. Một số cách xử trí khí SO2 hiệu quả hiện đang được áp dụng có thể kể đến như:
Tuy có hại nhưng do ứng dụng của khí SO2 là không hề nhỏ nên việc con người tiếp xúc và sử dụng loại khí này là điều cần thiết. Tuy nhiên, để đảm bảo an toàn, trong quá trình sử dụng cũng như bảo quản khí SO2 cần phải đặc biệt cẩn trọng. Luôn tuân thủ các quy tắc chung để việc sử dụng khí SO2 đạt hiệu quả tích cực nhất.
Trên đây LabVietChem vừa chia sẻ với các bạn một số thông tin cơ bản về các đặc tính lý – hóa cũng như ứng dụng của khí SO2. Hy vọng rằng bài viết hữu ích cho các bạn đang quan tâm tìm hiểu loại hợp chất này. Nếu cần thêm sự hỗ trợ, hãy liên hệ ngay với LabVietChem qua số điện thoại hotline 0826.020.020!
Hỗ trợ

Nguyễn Văn Trọng
Sales Director
094 6688 777
trongnguyen@labvietchem.vn

Cao Thu Hoài
Sales Engineer
0325 290 685
thietbi404@labvietchem.vn

Nguyễn Thúy Hảo
Sales Engineer
0364 841 980
nguyenhao@labvietchem.com.vn

Vũ Thị Thư
Sales Engineer
0326 046 889
vuthu@labvietchem.com.vn

Trần Thị Kim Mỵ
Sales Engineer
0348 140 389
sales@labvietchem.com.vn

Lưu Vân Quỳnh
Trưởng nhóm sinh hóa
0367 631 984
sales@labvietchem.com.vn

Phan Hải Phong
Sales Engineer
0949 966 821
sales@labvietchem.com.vn

Dương Tuấn Anh
Sales Engineer
0329 422 268
sales@labvietchem.com.vn

Hotline
Hóa chất và thiết bị thí nghiệm
0826 050 050
saleadmin806@vietchem.vn

Phạm Quang Phúc
Hóa chất và thiết bị thí nghiệm
0965 862 897
quangphuc@vietchem.vn

Hồ Thị Hoài Thương
Sales Engineer
0967 609 897
kd801@labvietchem.vn

Phạm Thị Nhật Hạ
Sales Engineer
0985 357 897
kd803@vietchem.vn

Vũ Thị Kim Khánh
Sales Engineer
0965 948 897
kd802@vietchem.vn

Trịnh Nhất Hậu
Kỹ thuật
0964 974 897
Service801@labvietchem.com

Trần Phương Bắc
Sales Engineer
0862 009 997
tranphuongbac@labvietchem.com.vn

Nguyễn Hoàng Giáo
Sales Engineer
0939 154 554
kd201@labvietchem.com.vn

Trần Công Sơn
Sales Engineer
090 105 1154
kd201@labvietchem.vn

Tạ Thảo Cương
Sales Engineer
0888851646
kd205@labvietchem.vn

Trần Thị Trúc Lil
Sales Engineer
0325 300 716
kd202@labvietchem.com.vn
Nhận xét đánh giá